Thuốc điều trị ung thư phổi Geftinat 250mg
Thuốc điều trị ung thư phổi Geftinat
Geftinat 250mg
Thành phần: Gefitinib 250mg
Viên nén bao phim: Hộp 1 vỉ x 30 viên.
Nhà sản xuất: NATCO PHARMA LIMITED
Xuất xứ: India
Thuốc Gefitinib có các biệt dược như: Geftinat; Iressa...
Đặc tính dược lực học
Nhóm dược lý trị liệu: Thuốc chống ung thư, ức chế protein kinase.
Cơ chế tác động và tác dụng dược lực:
- Yếu tố phát triển biểu bì (epidermal growth factor – EGF) và thụ thể (EGFR [HER1; ErbB1]) đóng vai trò chủ yếu trong quá trình phát triển và tăng sinh của tế bào bình thường và tế bào ung thư. Đột biến hoạt hóa EGFR trong tế bào ung thư là yếu tố quan trọng trong việc phát triển khối u, ngăn tế bào chết theo chương trình, tăng hình thành các mạch máu mới và thúc đẩy quá trình di căn của bướu.
- Gefitinib (Geftinat; Iressa...) là hoạt chất có phân tử nhỏ, ức chế chọn lọc tyrosin kinase (TKI) trên thụ thể của yếu tố phát triển biểu bì và điều trị hiệu quả ở bệnh nhân có khối u mang đột biến hoạt hóa của EGFR tyrosin kinase bất kể bước điều trị. Không có tác động lâm sàng liên quan ở bệnh nhân có khối u không mang đột biến EGFR.
- Đột biến hoạt hóa EGFR thường gặp (mất đoạn trên exon 19, L858R) có nhiều dữ liệu đáp ứng hỗ trợ cho nhạy cảm với Gefitinib (Geftinat; Iressa...); Ví dụ: Thời gian sống còn không tiến triển bệnh HR (95% Cl) 0,489 (0,336; 0,710) trong nhóm Gefitinib (Geftinat; Iressa...) so với nhóm hóa trị đôi [WJTOG3405]. Ít dữ liệu đáp ứng với Gefitinib (Geftinat; Iressa...) hơn ở các bệnh nhân có khối u chứa đột biến ít gặp, các dữ liệu sẵn có cho thấy G719X, L861Q và S7681 là các đột biến nhạy thuốc; và T790M đơn độc hoặc đột biến chèn đoạn ở exon 20 đơn độc là các cơ chế đề kháng thuốc.
- DNA của khối u trong hệ tuần hoàn (ctDNA)
Trong nghiên cứu lâm sàng IFUM, tình trạng đột biến được đánh giá trên mẫu khối u và mẫu ctDNA chiết tách từ huyết tương, bằng cách sử dụng bộ kít xét nghiệm Therascreen EGFR RGQ PCR (của hãng Qiagen). Cả hai mẫu ctDNA và mẫu khối u đều có thể đánh giá cho 652 bệnh nhân trong tổng số 1.060 bệnh nhân đã sàng lọc. Tỷ lệ đáp ứng khách quan của nhóm bệnh nhân có xét nghiệm đột biến dương tính trong cả mẫu khối u và mẫu ctDNA là 77% (95% CI: 66%-86%), và trong nhóm bệnh nhân chỉ có đột biến dương tính trên mẫu khối u là 60% (95% CI: 44%-74%).
- Bảng 1.
Các dữ liệu này cũng phù hợp với kết quả phân tích thăm dò định trước trong đề cương nghiên cứu. Trên phân nhóm bệnh nhân Nhật Bản trong nghiên cứu lâm sàng IPASS (Goto 2012). Trong nghiên cứu này, ctDNA chiết tách từ huyết thanh, không phải từ huyết tương, được dùng để phân tích đột biến EGFR sử dụng bộ kít EGFR Mutation Test Kit (DxS) (N=86). Trong nghiên cứu này, độ nhạy là 43,1%, độ đặc hiệu là 100%.
Độ an toàn và hiệu quả của thuốc trên lâm sàng
Điều trị bước 1
Trong một nghiên cứu lâm sàng ngẫu nhiên pha III về điều trị bước 1 trên bệnh nhân Châu Á ung thư phổi không tế bào nhỏ dạng tuyến tiến xa (giai đoạn IIIB hay IV), hút thuốc ít trước đây (ngưng hút thuốc ≥15 năm trước và hút ≤10 gói-năm) hoặc không bao giờ hút thuốc (Bảng 2).
1Trung Quốc, Hồng Kông, Indonesia, Nhật, Mã Lai, Philippines, Singapore, Đài Loan và Thái Lan.
Chất lượng sống khác nhau tùy thuộc vào tình trạng đột biến EGFR. Trong nhóm bệnh nhân có đột biến EGFR, nhiều bệnh nhân điều trị với Gefitinib (Geftinat; Iressa...) có sự cải thiện đáng kể về chất lượng cuộc sống và triệu chứng ung thư phổi so với carboplatin/paclitaxel (Bảng 3).
Trong nghiên cứu IPASS, Gefitinib (Geftinat; Iressa...) chứng minh hiệu quả vượt trội trên PFS, ORR, QOL và giảm triệu chứng mà không có sự khác biệt đáng kể về khả năng sống còn toàn bộ so với carboplatin/paclitaxel ở nhóm bệnh nhân chưa được điều trị trước đó, bị bệnh ung thư phổi loại không phải tế bào nhỏ tiến triển tại chỗ hay di căn, các khối u này có đột biến hoạt hóa EGFR tyrosin kinase.
Trên các bệnh nhân đã được điều trị trước đó
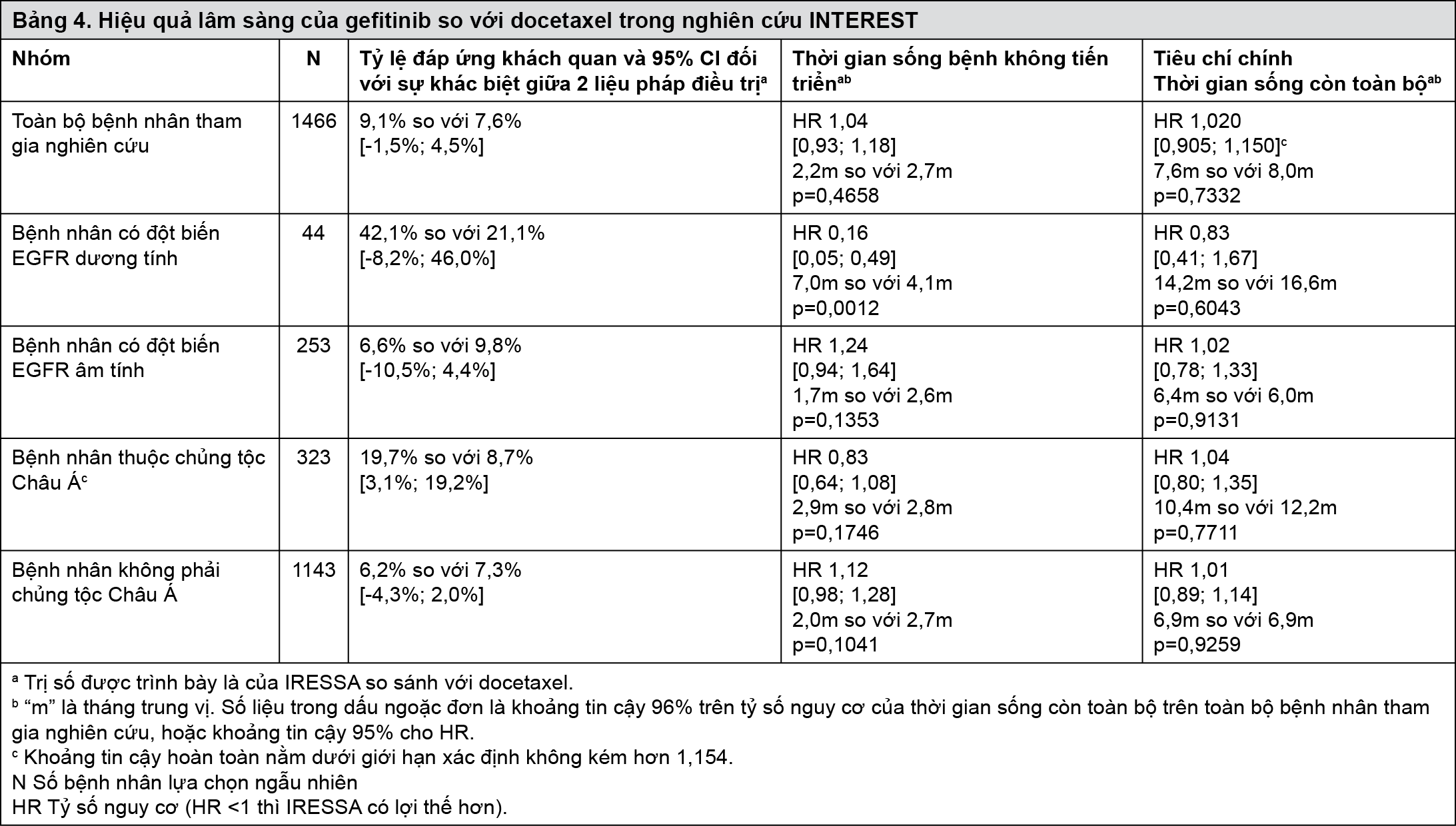
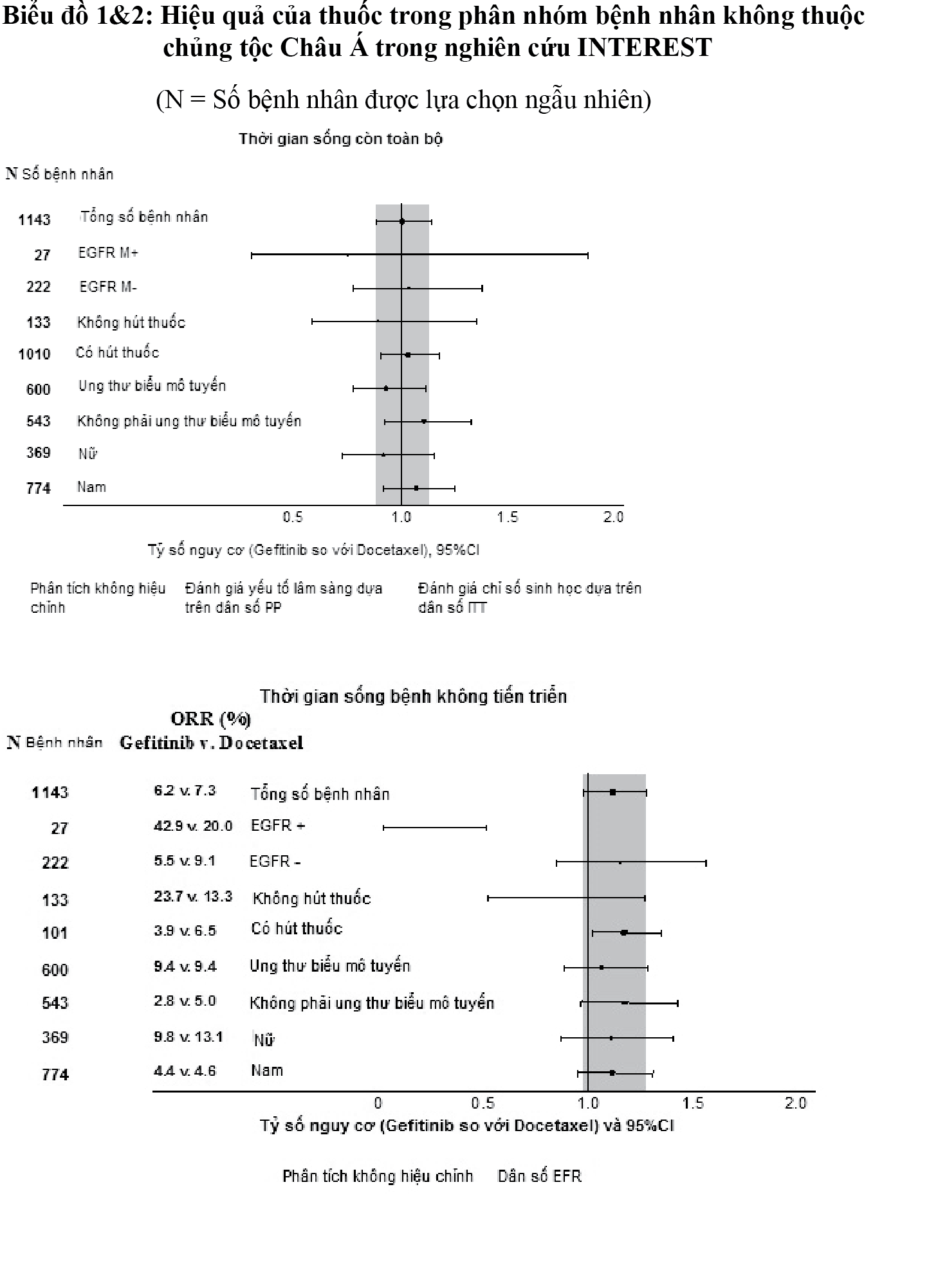
Trong một nghiên cứu lâm sàng pha III (INTEREST) tiến hành ngẫu nhiên trên bệnh nhân NSCLC giai đoạn tiến triển tại chỗ hoặc di căn mà trước đây đã dùng hóa trị có platinum. Trên toàn bộ bệnh nhân tham gia nghiên cứu, không có sự khác biệt có ý nghĩa thống kê giữa Gefitinib (Geftinat; Iressa...) và docetaxel (75mg/m2) về thời gian sống còn toàn bộ, thời gian sống bệnh không tiến triển và tỷ lệ đáp ứng khách quan (Bảng 4).
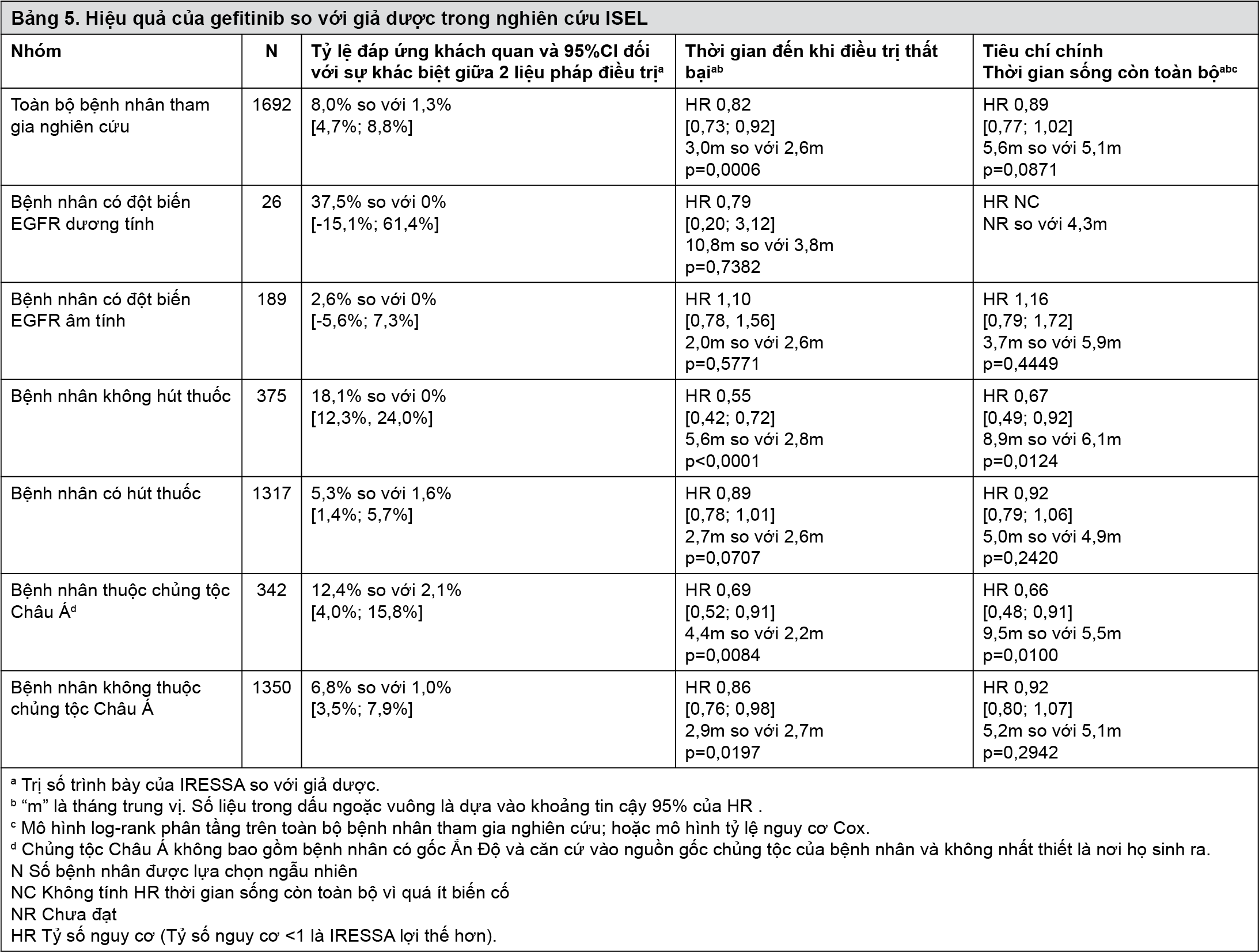
- Nghiên cứu lâm sàng pha III (ISEL) thực hiện ngẫu nhiên trên bệnh nhân NSCLC tiến triển mà đã dùng 1 hoặc 2 phác đồ hóa trị trước đó và đã kháng trị hoặc không dung nạp với phác đồ điều trị gần nhất. Gefitinib (Geftinat; Iressa...) phối hợp với liệu pháp chăm sóc nâng đỡ (BSC: Best Supportive Care) được so sánh với giả dược phối hợp với liệu pháp chăm sóc nâng đỡ. Gefitinib (Geftinat; Iressa...) không làm kéo dài đáng kể thời gian sống còn trên toàn bộ bệnh nhân tham gia nghiên cứu. Thời gian sống còn khác nhau tùy theo tình trạng hút thuốc và yếu tố chủng tộc (Bảng 5).
- Nghiên cứu IFUM là nghiên cứu đa trung tâm, đơn nhánh, tiến hành trên các bệnh nhân da trắng (n=106) bị ung thư phổi không tế bào nhỏ có đột biến EGFR nhạy cảm hoạt hóa để khẳng định rằng hoạt tính của Gefitinib (Geftinat; Iressa...) ở bệnh nhân da trắng và bệnh nhân Châu Á là tương tự nhau. Theo đánh giá của nghiên cứu viên, trị số ORR là 70% và trung vị PFS là 9,7 tháng. Các dữ liệu này cũng tương tự như các dữ liệu báo cáo trong nghiên cứu IPASS.
Tình trạng đột biến EGFR và đặc tính lâm sàng
Đặc điểm lâm sàng của bệnh nhân nữ, không hút thuốc, ung thư dạng tuyến cho thấy là yếu tố tiên đoán độc lập về tình trạng đột biến EGFR dương tính trong một phân tích đa biến của 786 bệnh nhân da trắng từ các nghiên cứu Gefitinib (Geftinat; Iressa...)* (Bảng 6). Bệnh nhân châu Á cũng có một tỷ lệ khối u đột biến dương tính cao hơn.
Đặc tính dược động học
- Hấp thu: Sau khi uống Gefitinib (Geftinat; Iressa...), sự hấp thu tương đối chậm và nồng độ đỉnh Gefitinib (Geftinat; Iressa...) trong huyết tương đạt từ 3-7 giờ sau khi uống thuốc. Sinh khả dụng tuyệt đối trung bình là 59% ở bệnh nhân ung thư. Thức ăn không làm thay đổi đáng kể nồng độ Gefitinib (Geftinat; Iressa...) trong cơ thể. Trong một thử nghiệm trên người tình nguyện khoẻ mạnh có độ pH dịch vị duy trì >5, nồng độ Gefitinib (Geftinat; Iressa...) trong cơ thể giảm 47%, có thể là do giảm độ hòa tan của Gefitinib (Geftinat; Iressa...) ở dạ dày (xem phần ''Cảnh báo'' và ”Tương tác”).
- Phân bố: Thể tích phân bố trung bình của Gefitinib (Geftinat; Iressa...) ở trạng thái hằng định là 1400 lít, chứng tỏ là thuốc phân bố rộng rãi vào các mô. Khoảng 90% thuốc gắn kết với protein huyết tương. Gefitinib (Geftinat; Iressa...) gắn kết với albumin và α1-acid glycoprotein trong huyết thanh.
Dữ liệu in vitro cho thấy rằng Gefitinib (Geftinat; Iressa...) là chất nền cho sự vận chuyển qua màng tế bào của protein Pgp.
- Chuyển hóa:
Dữ liệu in vitro cho thấy rằng CYP3A4 và CYD2D6 là isozym P450 chính có liên quan đến quá trình chuyển hóa oxy hóa của Gefitinib (Geftinat; Iressa...).
Các nghiên cứu in vitro đã chứng tỏ Gefitinib (Geftinat; Iressa...) ít có khả năng ức chế CYP2D6. Gefitinib (Geftinat; Iressa...) cho thấy không có tác động cảm ứng enzym trong các nghiên cứu ở động vật và không ức chế đáng kể (in vitro) trên bất kỳ cytochrom P450 enzym.
Gefitinib (Geftinat; Iressa...) được chuyển hóa rộng rãi ở người. 5 chất chuyển hóa đã được nhận biết đầy đủ trong phân và 8 chất chuyển hóa trong huyết tương ở người. Chất chuyển hóa chính được định danh là O-desmethyl Gefitinib (Geftinat; Iressa...), hoạt tính kém 14 lần so với Gefitinib (Geftinat; Iressa...) về khả năng ức chế sự phát triển tế bào được kích hoạt bởi EGFR và không có tác động ức chế sự phát triển tế bào khối u ở chuột. Vì vậy, chất chuyển hóa này được xem như không đóng góp vào tác động lâm sàng của Gefitinib (Geftinat; Iressa...).
- In vitro, O-desmethyl Gefitinib (Geftinat; Iressa...) đã được chứng minh là sản sinh qua men CYP2D6. Vai trò của men CYP2D6 trong quá trình thanh thải chuyển hóa Gefitinib (Geftinat; Iressa...) đã được đánh giá trong một nghiên cứu lâm sàng trên người tình nguyện khỏe mạnh đã khảo sát kiểu gen về tình trạng CYP2D6 (genotyped for CYP2D6 status). Ở người chuyển hóa kém, không phát hiện O-desmethyl Gefitinib (Geftinat; Iressa...) được sản sinh ở mức độ có thể đo lường được. Nồng độ và thời gian tiếp xúc với Gefitinib (Geftinat; Iressa...) trong máu ở cả nhóm chuyển hóa mạnh và nhóm chuyển hóa kém đều biến thiên rộng và trùng lắp nhau nhưng nồng độ và thời gian tiếp xúc trung bình với Gefitinib (Geftinat; Iressa...) trong máu ở nhóm chuyển hóa kém thì cao gấp đôi. Hiện tượng người không có CYP2D6 có nồng độ thuốc và thời gian tiếp xúc với thuốc trong máu cao hơn có thể có ý nghĩa lâm sàng vì đã gặp các phản ứng ngoại ý liên quan đến liều và nồng độ thuốc trong cơ thể.
- Thải trừ:
Gefitinib (Geftinat; Iressa...) được bài tiết chủ yếu dưới dạng chất chuyển hóa qua phân, độ thải trừ thuốc và các chất chuyển hóa qua thận ít hơn 4% liều dùng.
Tổng thanh thải Gefitinib (Geftinat; Iressa...) trong huyết tương là khoảng 500 ml/phút và trung bình thời gian bán thải cuối là 41 giờ ở bệnh nhân ung thư. Uống Gefitinib (Geftinat; Iressa...) một lần mỗi ngày sẽ dẫn đến tích lũy thuốc từ 2 đến 8 lần, với nồng độ và thời gian tiếp xúc ở trạng thái ổn định đạt được sau 7-10 liều dùng. Ở trạng thái ổn định, nồng độ thuốc trong huyết tương tuần hoàn được duy trì gấp 2-3 lần với khoảng cách liều 24 giờ.
- Các nhóm dân số đặc biệt: Khi phân tích dữ liệu dựa trên nhóm dân số ở bệnh nhân ung thư, không xác định có mối liên hệ giữa nồng độ đáy ở trạng thái ổn định đã tiên đoán trước (predicted steady state trough concentration) và độ tuổi bệnh nhân, thể trọng, giới tính, chủng tộc hoặc độ thanh thải creatinin (>20 ml/phút).
- Suy gan:
Trong một nghiên cứu nhãn mở pha I dùng liều đơn Gefitinib (Geftinat; Iressa...) 250 mg trên bệnh nhân suy gan nặng, trung bình hoặc nhẹ do xơ gan (theo phân loại Child-Pugh), đã có sự gia tăng về nồng độ thuốc trong máu trong tất cả nhóm so với nhóm chứng khỏe mạnh. Đã ghi nhận có mức độ phơi nhiễm với Gefitinib (Geftinat; Iressa...) tăng trung bình gấp 3,1 lần ở bệnh nhân suy gan trung bình và nặng. Không có bệnh nhân nào bị ung thư, tất cả đều bị xơ gan và vài người bị viêm gan. Sự tăng mức phơi nhiễm này có ý nghĩa lâm sàng vì đã gặp các phản ứng ngoại ý liên quan đến liều và mức phơi nhiễm với thuốc trong cơ thể.
Gefitinib (Geftinat; Iressa...) đã được đánh giá trong một thử nghiệm lâm sàng thực hiện trên 41 bệnh nhân có bướu đặc (solid tumour) và chức năng gan bình thường, suy chức năng gan trung bình hoặc nặng (phân loại Tiêu chuẩn Đánh giá Độc tính Thường gặp dựa vào AST, alkalin phosphatase và bilirubin) do di căn gan. Kết quả cho thấy sau khi dùng liều hàng ngày Gefitinib (Geftinat; Iressa...) 250 mg, các trị số như thời gian đạt nồng độ ổn định trong máu, tổng độ thanh thải huyết tương và mức tiếp xúc ở trạng thái ổn định (Cmaxss, AUC24ss) tương tự ở các nhóm có chức năng gan bình thường và chức năng gan suy giảm mức độ trung bình. Dữ liệu của 4 bệnh nhân có chức năng gan rối loạn trầm trọng do di căn gan cho thấy mức phơi nhiễm ở trạng thái ổn định của các bệnh nhân này cũng tương tự như ở bệnh nhân có chức năng gan bình thường.
Chỉ định/Công dụng: Gefitinib (Geftinat; Iressa...) được chỉ định điều trị cho bệnh nhân người lớn ung thư phổi loại không phải tế bào nhỏ giai đoạn tiến triển tại chỗ hoặc di căn mà có đột biến hoạt hóa EGFR TK.
Việc điều trị với Gefitinib (Geftinat; Iressa...) nên được tiến hành và theo dõi bởi các bác sỹ có kinh nghiệm trong điều trị ung thư.
Liều khuyến cáo Gefitinib (Geftinat; Iressa...) là 1 viên 250 mg, ngày 1 lần. Nếu quên dùng 1 liều thuốc, nên uống ngay khi nhớ ra. Nếu việc quên uống thuốc dưới 12 giờ tính đến thời điểm dùng liều kế tiếp, bệnh nhân không nên dùng liều thuốc đã lỡ quên uống. Bệnh nhân không nên dùng liều gấp đôi (uống cùng lúc 2 liều thuốc) để bù cho liều đã quên uống.
- Trẻ em: Độ an toàn và hiệu quả của Gefitinib (Geftinat; Iressa...) ở trẻ em và thiếu niên dưới 18 tuổi chưa được thiết lập. Chưa có sử dụng Gefitinib (Geftinat; Iressa...) trên trẻ em với chỉ định ung thư phổi loại không phải tế bào nhỏ.
- Suy gan: Bệnh nhân suy gan trung bình đến nặng (Child Pugh B hoặc C) do xơ gan có tăng nồng độ Gefitinib (Geftinat; Iressa...) trong huyết tương. Nên theo dõi chặt chẽ các phản ứng ngoại ý ở các bệnh nhân này. Nồng độ trong huyết tương không tăng ở bệnh nhân có tăng aspartat transaminase (AST), alkalin phosphatase hoặc bilirubin do di căn gan (xem phần “Đặc tính dược động học”).
- Suy thận: Không cần điều chỉnh liều ở bệnh nhân suy giảm chức năng thận có độ thanh thải creatinin >20 ml/phút. Có rất ít số liệu ở bệnh nhân có độ thanh thải creatinin ≤20 ml/phút và cần thận trọng khi sử dụng thuốc ở nhóm bệnh nhân này (xem phần “Đặc tính dược động học”).
- Bệnh nhân cao tuổi: Không cần điều chỉnh liều dựa vào lứa tuổi của bệnh nhân (xem phần “Đặc tính dược lực học”).
- Bệnh nhân có suy giảm enzym CYP2D6: Không có khuyến cáo chỉnh liều cụ thể ở bệnh nhân có kiểu gen chuyển hóa qua CYP2D6 giảm, nhưng ở các bệnh nhân này nên được theo dõi chặt chẽ các phản ứng ngoại ý (xem phần “Đặc tính dược lực học”).
- Điều chỉnh liều khi có độc tính của thuốc: Bệnh nhân bị tiêu chảy hoặc có phản ứng ngoại ý trên da mà không dung nạp có thể được kiểm soát thành công khi ngưng dùng thuốc trong một thời gian ngắn (≤14 ngày) và sau đó dùng trở lại liều 250 mg (xem phần “Tác dụng ngoại ý”). Đối với bệnh nhân không thể dung nạp thuốc sau một đợt ngắt quãng điều trị, nên ngưng sử dụng Gefitinib (Geftinat; Iressa...) và cân nhắc phương pháp điều trị thay thế.
Cách dùng:
Có thể uống thuốc trong hoặc ngoài bữa ăn, cùng một thời gian trong ngày. Thuốc có thể được nuốt nguyên viên cùng với một ít nước hoặc trường hợp không thể uống nguyên viên thuốc thì có thể phân tán viên thuốc trong nước. Nên thả viên thuốc trong nửa ly nước uống (không chứa carbonat). Không nên dùng chung với các thức uống khác. Không được nghiền viên thuốc, thả nguyên viên thuốc trong nửa ly nước. Khuấy đều cho đến khi viên thuốc phân tán hoàn toàn (khoảng 20 phút) và uống dịch thuốc ngay lập tức sau khi thuốc phân tán hoàn toàn (nghĩa là trong vòng 60 phút). Tráng ly với nửa ly nước và uống. Dịch thuốc phân tán cũng có thể được dùng qua ống thông mũi-dạ dày hoặc ống thông dạ dày
- Thận trọng: Khi xem xét sử dụng Gefitinib (Geftinat; Iressa...) để điều trị cho bệnh nhân ung thư phổi loại không phải tế bào nhỏ giai đoạn tiến triển hoặc di căn, khuyến cáo xét nghiệm đánh giá đột biến EGFR tại mô khối u cho tất cả các bệnh nhân. Nếu mẫu khối u không thể đánh giá được, thì có thể sử dụng mẫu DNA của khối u trong hệ tuần hoàn (ctDNA) thu thập từ mẫu máu (huyết tương). Chỉ dùng các phương pháp xét nghiệm có độ tái lặp, độ tin cậy, độ nhạy cùng với tiện ích đã được chứng minh về xác định tình trạng đột biến EGFR của khối u hay ctDNA để tránh kết quả âm tính giả hay dương tính giả (xem phần Đặc tính dược lực học).
- Bệnh phổi mô kẽ (ILD)
Bệnh phổi mô kẽ, có thể khởi phát cấp tính, đã được quan sát thấy ở 1,3% bệnh nhân đang dùng Gefitinib (Geftinat; Iressa...), và một vài trường hợp có thể bị tử vong (xem phần Tác dụng ngoại ý). Nếu bệnh nhân có biểu hiện xấu đi với các triệu chứng hô hấp như khó thở, ho và sốt, nên ngừng Gefitinib (Geftinat; Iressa...) và cho kiểm tra ngay. Nếu xác nhận chẩn đoán là bệnh phổi mô kẽ, nên ngưng dùng Gefitinib (Geftinat; Iressa...) và điều trị bệnh nhân bằng các biện pháp thích hợp.
- Trong một nghiên cứu dược lý dịch tễ có đối chứng tại Nhật thực hiện trên 3.159 bệnh nhân ung thư phổi loại không tế bào nhỏ (NSCLC) đã được theo dõi trong 12 tuần khi dùng Gefitinib (Geftinat; Iressa...) hoặc hóa trị, các yếu tố nguy cơ phát triển bệnh phổi mô kẽ (ILD) như sau đã được xác định (bất kể bệnh nhân dùng Gefitinib (Geftinat; Iressa...) hoặc hóa trị) là: Hút thuốc, tình trạng thể chất kém (PS ≥2), giảm thể tích phổi bình thường có chứng cứ chụp cắt lớp CT (≤ 50%), mới được chẩn đoán NSCLC (<6 tháng), bệnh phổi mô kẽ (ILD) có sẵn trước, lớn tuổi (≥55 tuổi) và bệnh tim đồng thời. Đã ghi nhận gia tăng nguy cơ bệnh phổi mô kẽ ở nhóm dùng Gefitinib (Geftinat; Iressa...) so với hóa trị chủ yếu trong vòng 4 tuần đầu sử dụng (giá trị OR hiệu chỉnh 3,8; 95% Cl 1,9-7,7); sau đó nguy cơ tương đối thấp hơn (giá trị OR hiệu chỉnh 2,5; 95% Cl 1,1-5,8). Trong số bệnh nhân bị ILD ở cả 2 nhóm Gefitinib (Geftinat; Iressa...) và hóa trị thì nguy cơ tử vong cao ở nhóm bệnh nhân có các yếu tố nguy cơ sau: Hút thuốc, giảm thể tích phổi bình thường có chứng cứ chụp cắt lớp CT (≤ 50%), bệnh phổi mô kẽ (ILD) có sẵn trước, lớn tuổi (≥65 tuổi) và các vùng dính liền với màng phổi quá rộng (≥ 50%).
- Ngộ độc gan và suy giảm chức năng gan
Bất thường xét nghiệm chức năng gan (bao gồm tăng alanin aminotransferase, aspartat aminotransferase, bilirubin) đã được ghi nhận nhưng ít khi có biểu hiện viêm gan (xem phần ”Tác dụng ngoại ý”). Vài báo cáo riêng lẻ suy chức năng gan mà một số trường hợp dẫn đến tử vong. Vì vậy, bệnh nhân được khuyến cáo nên kiểm tra chức năng gan định kỳ. Gefitinib (Geftinat; Iressa...) nên được dùng thận trọng trên bệnh nhân có thay đổi chức năng gan ở mức độ nhẹ hoặc trung bình. Cân nhắc ngưng sử dụng thuốc nếu các thay đổi là nghiêm trọng.
Suy giảm chức năng gan do xơ gan đã được ghi nhận là dẫn đến tăng nồng độ Gefitinib (Geftinat; Iressa...) trong huyết tương (xem phần “Đặc tính dược lực học”).
- Tương tác với các thuốc khác
Các chất gây cảm ứng với hệ enzym CYP3A4 có thể làm tăng chuyển hóa Gefitinib (Geftinat; Iressa...) và giảm nồng độ Gefitinib (Geftinat; Iressa...) trong huyết tương. Vì vậy, khi phối hợp với các chất gây cảm ứng CYP3A4 (như phenytoin, carbamazepin, rifampicin, barbiturat hoặc chế phẩm từ dược liệu có chứa St John’s Wort/Hypericum perforatum) có thể làm giảm hiệu lực của thuốc và vì thế nên tránh sử dụng chung các thuốc này (xem phần Tương tác).
Ở các bệnh nhân có kiểu gen chuyển hóa qua CYP2D6 giảm, điều trị bằng thuốc ức chế mạnh CYP3A4 có thể dẫn đến tăng nồng độ của Gefitinib (Geftinat; Iressa...) trong huyết tương. Khi bắt đầu điều trị bằng thuốc ức chế CYP3A4, bệnh nhân cần được theo dõi chặt chẽ các phản ứng ngoại ý của Gefitinib (Geftinat; Iressa...) (xem phần "Tương tác").
Tăng INR (International Normalised Ratio) và/hoặc các biến cố xuất huyết đã được báo cáo ở một số bệnh nhân đang dùng warfarin (xem phần “Tương tác”). Nên thường xuyên theo dõi sự thay đổi về thời gian prothrombin (PT) hoặc INR ở bệnh nhân đang dùng warfarin.
Các thuốc làm tăng đáng kể và kéo dài độ pH dịch vị như thuốc ức chế bơm proton và thuốc đối kháng thụ thể H2 có thể làm giảm sinh khả dụng và nồng độ Gefitinib (Geftinat; Iressa...) trong huyết tương và vì thế có thể giảm hiệu lực của thuốc. Thuốc kháng acid nếu dùng thường xuyên gần thời điểm uống thuốc Gefitinib (Geftinat; Iressa...) có thể có tác động tương tự (xem phần “Tương tác” và “Đặc tính Dược động học”).
Dữ liệu từ các nghiên cứu lâm sàng pha II, khi dùng đồng thời Gefitinib (Geftinat; Iressa...) và vinorelbin cho thấy Gefitinib (Geftinat; Iressa...) có thể làm tăng tác động giảm bạch cầu trung tính của vinorelbin.
Lactose: Gefitinib (Geftinat; Iressa...) có chứa lactose. Bệnh nhân có vấn đề di truyền hiếm gặp kém dung nạp galactose, thiếu hụt Lapp lactose hoặc kém hấp thu glucose-galactose thì không nên dùng thuốc này.
Các thận trọng khác
Nên khuyên bệnh nhân khám bác sỹ ngay lập tức khi có tiêu chảy trầm trọng hoặc dai dẳng, buồn nôn, nôn hoặc biếng ăn mà có thể gián tiếp dẫn tới mất nước cơ thể. Các triệu chứng này có thể được xử trí theo bệnh cảnh lâm sàng (xem phần Tác dụng ngoại ý).
Bệnh nhân có các dấu hiệu và triệu chứng nghi ngờ viêm giác mạc như tình trạng cấp tính hay trầm trọng hơn: viêm mắt, tuyến lệ, mẫn cảm với ánh sáng, nhìn mờ, đau mắt và/hoặc đỏ mắt nên nhanh chóng tham vấn bác sĩ chuyên khoa mắt.
Nếu chẩn đoán đã xác định là viêm loét giác mạc, nên ngưng điều trị với Gefitinib (Geftinat; Iressa...) và nếu các triệu chứng không hết hẳn hoặc tái phát khi sử dụng lại Gefitinib (Geftinat; Iressa...), cân nhắc ngưng sử dụng lâu dài Gefitinib (Geftinat; Iressa...).
Trong một nghiên cứu pha I/II sử dụng Gefitinib (Geftinat; Iressa...) và xạ trị ở bệnh nhân nhi mới được chẩn đoán u thần kinh đệm cuống não (brain stem glioma) hoặc u thần kinh đệm ác tính trên lều đã được cắt bỏ không hoàn toàn (incompletely resected supratentorial malignant glioma), có 4 trường hợp xuất huyết ở hệ thần kinh trung ương (trong đó có 1 trường hợp tử vong) đã được ghi nhận trong 45 bệnh nhân tham gia nghiên cứu. Một trường hợp xuất huyết ở hệ thần kinh trung ương ở trẻ u màng não thất (ependymoma) cũng được ghi nhận trong thử nghiệm dùng Gefitinib (Geftinat; Iressa...) đơn thuần. Việc tăng nguy cơ xuất huyết não ở bệnh nhân trưởng thành bị ung thư phổi loại không phải tế bào nhỏ dùng Gefitinib (Geftinat; Iressa...) chưa được thiết lập.
Đã có ghi nhận thủng dạ dày ruột ở bệnh nhân dùng Gefitinib (Geftinat; Iressa...). Trong đa số các trường hợp, điều này có liên quan đến các yếu tố nguy cơ đã biết khác, bao gồm tuổi cao, sử dụng đồng thời các thuốc khác như steroid, kháng viêm NSAID, bệnh nền loét dạ dày ruột, hút thuốc hoặc di căn ở ruột tại vị trí thủng.
- Ảnh hưởng trên khả năng lái xe và vận hành máy móc: Đã có báo cáo về triệu chứng suy nhược trong khi điều trị bằng Gefitinib (Geftinat; Iressa...). Do đó, các bệnh nhân có triệu chứng này nên thận trọng khi lái xe hoặc vận hành máy.
- Quá Liều: Không có trị liệu đặc biệt trong trường hợp dùng quá liều Gefitinib (Geftinat; Iressa...). Tuy nhiên, trong nghiên cứu lâm sàng pha I, một số ít bệnh nhân đã được điều trị bằng liều lên đến 1000 mg/ngày. Đã ghi nhận sự tăng tần suất và mức độ trầm trọng của một số phản ứng ngoại ý, chủ yếu là tiêu chảy và ban da. Các phản ứng ngoại ý do dùng quá liều nên được điều trị triệu chứng; đặc biệt tình trạng tiêu chảy nặng nên được điều trị theo chỉ định lâm sàng. Trong một nghiên cứu với số lượng giới hạn bệnh nhân được điều trị hàng tuần với liều từ 1500 mg đến 3500 mg. Trong nghiên cứu này, nồng độ và thời gian tiếp xúc với Gefitinib (Geftinat; Iressa...) không tăng cùng với liều, các phản ứng ngoại ý chủ yếu ở mức độ nhẹ đến trung bình và phù hợp với các dữ liệu an toàn thuốc Gefitinib (Geftinat; Iressa...) đã biết.
- Quá mẫn với hoạt chất hay tá dược của thuốc.
- Phụ nữ trong độ tuổi sinh sản: Khuyến cáo phụ nữ trong &
Thuốc Sorafenat 200mg
Tên Thuốc: Sorafenat 200mg Thành phần: Sorafenib 200mg Viên nén: Hoạt chất Sorafenib 200 mg Quy cách đóng gói: Hộp 120 viên Nhà sản xuất: Natco Pharma Xuất xứ: Ấn Độ
Thuốc Tagrix 80mg
Tên thương mại: Tagrix 80mg Thành phần: Osimertinib Hàm lượng: 80mg Dạng: Viên nén Đóng gói: Hộp chữ nhật 30 viên Nhà phân phối: Beacon Pharma Ltd
Thuốc Erlonat 150mg
2.000.000đ
- Tên thuốc: Erlonat 150mg - Nhà sản xuất: NATCO PHARMA LIMITED - Xuất xứ: India - Thành phần: Erlotinib 150mg (Biệt dược của Erlotinib như: Erlonat; Erlocip; Erlotib, Tarceva; Zyceva ...) - Dạng bào chế: Viên nén 150mg - Đóng gói: Hộp dạng vỉ 30 viên
Thuốc Osicent 80mg
Tên thương mại: Osicent 80mg Thành phần: Osimertinib Hàm lượng: 80mg Dạng: Viên nén Đóng gói: Hộp giấy chứa lọ 30 viên Nhà phân phối: Incepta Pharmaceuticals Ltd., Xuất xứ: Bangladesh Thuốc Osicent mua ở đâu giá rẻ nhất và uy tín nhất? Chúng tôi là đơn vị cung cấp thuốc Osicent 80mg chính hãng trên toàn quốc. Hãy gọi 0966.58.1290
Thuốc Osimert 80mg
Tên Thuốc: Osimert 80mg Thành phần: Osimertinib 80mg (dạng viên nén) Hộp: 30 viên nén Nhà sản xuất: Everest Pharmaceuticals Ltd., Xuất xứ: Bangladesh
Thuốc Hepbest 25mg
500.000đ
Tên thuốc: HepBest 25mg Thành phần, hàm lượng: Mỗi viên nén bao phim có chứa Tenofovir Alafenamide 25 mg Dạng bào chế: Viên nén bao phim; hình thuôn dài màu trắng hoặc ngà trắng có khắc chữ M ở một mặt và chữ TFI ở mặt còn lại. Đóng gói: Hộp 30 viên. Nhà sản xuất: Mylan Laboratories Limited Xuất xứ: Ấn Độ
Thuốc Alecensa 150mg
Hãng sản xuất: Roche Tên thương mại: Alecensa 150mg Thành phần: Alectinib 150mg Hàm lượng: 150mg Dạng: Viên nhộng Đóng gói: Hộp 224 viên bên trong chứa 4 hộp nhỏ 56 viên Nhà phân phối: Roche - Thổ Nhĩ Kỳ
Thuốc Crizonix 250mg
- Tên thương hiệu: Crizonix 250mg - Thành phần: Crizotinib 250mg - Hàm lượng: 250mg - Dạng: Viên con nhộng - Đóng gói: Hộp 60 viên - Nhà sản xuất: Beacon Pharmaceuticals Limited... - Xuất sứ: Bangladesh.
Thuốc IRESSA 250 mg
Tên thương mại: IRESSA 250mg Thành phần: Gefitinib Dạng: Viên nén bao phim Nhà sản xuất: AstraZeneca
Thuốc Nexavar 200mg
Tên thuốc: Nexavar 200mg Thành phần: Sorafenib 200mg Viên nén: 200 mg
Thuốc Afanix 40mg
Tên thuốc: Afanix 40mg Thành phần: Afatinib 40mg Viên nén: 40mg Đóng gói hộp: 30 viên (đủ dùng cho 1 tháng điều trị) Nhà sản xuất: BEACON Pharmaceuticals Limited Xuất xứ: Bangladesh
Thuốc Luciosim 80mg
Tên thuốc: LUCIOSIM 80mg Thành phần: Osimertinib 80mg Osimertinib có các biệt dược như: Luciosim, Osimert, Tagrix, Tagrisso, Osicent.... Viên nén: 80mg Đóng gói lọ/hũ: 30 viên (Đủ dùng điều trị 1 tháng) Nhà sản xuất: LUCIUS pharmaceuticals. Xuất xứ: Colombo
Thuốc Noxalk 150mg
Thành phần: Ceritinib 150mg Viên nang: 150 mg Nhà sản xuất: NATCO PHARMA LIMITED Xuất xứ: India Đóng gói: 30 viên/Hộp
Thuốc Tarceva 150mg
Nhà chế tạo: Roche Thành phần: Erlotinib 150mg
Thuốc Tykerb 250mg
Tên thuốc: Tykerb 250mg Thành phần: Lapatinib Viên nén: 250mg
Thuốc Xbira (Abirateron) 250mg
Thành phần: Abirateron acetat 250mg. Đóng gói: Hộp 1 lọ 120 viên nén. Nhà sản xuất: Công ty Dược phẩm Cipla. Xuất xứ: Ấn Độ.
Thuốc Cabozanix/Cabozatinib
Tên thuốc: Cabozanix Thành phần: Cabozantinib Đóng gói: 30 viên/hộp Xuất xứ: Bangladesh
Thuốc Kadcyla
- Tên thuốc: Kadcyla -Thành phần: Trastuzumab emtansine - Mỗi lọ: Trastuzumab emtansin 100mg hoặc 160mg
Thuốc Avastin
Tên thuốc: Avastin Thành phần: Avastin (bevacizumab)
Okinawa Fucoidan Kanehide Bio 180 viên (Fucoidan-xanh)
1.500.000đ
- Tên sản phẩm: Okinawa Fucoidan Kanehide Bio - Hàm lượng: 295 mg/viên - Mỗi viên chứa: 235 mg Fucoidan nguyên chất - Nhà sản xuất: Kanehide Biotechnology Co., Ltd. - Xuất xứ: Okinawa - Nhật Bản - Đóng gói: 180 viên/Lọ - Dạng bào chế: Viên nang


























Xem thêm